Cultura e scienze
Tumore al seno, la scoperta su test genetici e chirurgia preventiva
Giovanni Drogo 29/03/2018
È del ricercatore italiano Fabio Girardi uno degli ultimi contributi alla ricerca epidemiologica nella prevenzione del tumore mammario/ovarico ereditario pubblicato sulla rivista Genetics in Medicine dove si dimostra che donne prive della mutazione BRCA1/BRCA2 (quella di Angelina Jolie) presente nella loro famiglia non hanno un rischio aumentato di tumore mammario od ovarico rispetto alla popolazione generale e quindi non devono per forza sottoporsi all’intervento chirurgico

Il grande pubblico ha scoperto dell’esistenza dei geni BRCA1 e BRCA2 e dei rischi connessi alle loro eventuali mutazioni grazie ad Angelina Jolie. L’attrice holliwoodiana si è infatti sottoposta (nel 2013 e nel 2015) a due interventi chirurgici (una doppia mastectomia e l’asportazione delle ovaie) dopo aver effettuato un test genetico ed aver scoperto di essere affetta da una mutazione del gene BRCA1. Secondo i medici consultati da Angelina Jolie il gene difettoso aumentava dell’87% il rischio di contrarre un cancro al seno e del 50% quello di un tumore alle ovaie. Una scelta radicale dettata anche dal fatto che la madre di Angelina Jolie, la nonna e la zia sono infatti tutte e tre morte per cancro alle ovaie. Nel caso della Jolie siamo in presenza di due fattori: la mutazione genetica e una familiarità. Cosa succede invece quando c’è la familiarità ma il test genetico è negativo?
Cosa comportano le mutazioni sui geni BRCA1 e BRCA2
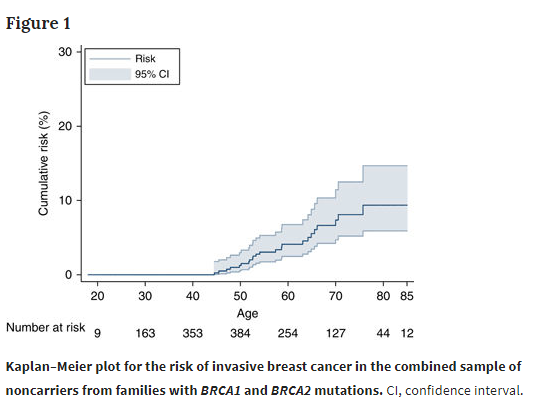
Uno studio condotto da Fabio Girardi del Centre for Cancer Genetic Epidemiology dell’Università di Cambridge ha dimostrato che donne prive della mutazione BRCA1/BRCA2 presente in alcuni familiari non hanno un rischio aumentato di tumore mammario od ovarico rispetto alla popolazione generale.Lo studio dal titolo Risks of breast or ovarian cancer in BRCA1 or BRCA2 predictive test negatives: findings from the EMBRACE study è stato pubblicato sulla rivista Genetics in Medicine ( pubblicazione che fa parte del gruppo Nature), il giornale ufficiale dell’American College of Medical Genetics and Genomics. Girardi è un giovane medico italiano (di Castelfranco Veneto) che si è specializzato in Oncologia Medica a Padova, successivamente si è laureato in Epidemiologia a Cambridge e attualmente è studente di dottorato presso la London School of Hygiene and Tropical Medicine di Londra ma rifiuta di essere definito “cervello in fuga” perché in Inghilterra ci è andato per perfezionare la sua formazione e vorrebbe prima o poi tornare in Italia.

Lo Strangeways Research Laboratory a Cambridge che ospita il gruppo di ricerca di cui fa parte Girardi
La chirurgia preventiva non è sempre consigliabile
Lo studio epidemologico condotto da Girardi non riguarda il trattamento del tumore mammario o di quello alle ovaie ma analizza, prendendo in esame i dati epidemiologici forniti dai partecipanti allo studio Epidemiological Study of Familial Breast Cancer (EMBRACE), il rischio delle donne che sono risultate negative ai test genetici pur avendo una familiarità. I partecipanti sono stati reclutati a partire dal 1997 attraverso i centri regionali britannici che svolgono i test genetici sul cancro. Inoltre lo studio si è avvalso di BOADICEA un algoritmo statistico che consente di calcolare il rischio di tumore mammario e ovarico sulla base di mutazioni note o anche della sola storia familiare. Pur essendo lo studio condotto in donne familiari di pazienti BRCA1/BRCA2 positive, queste rappresentano una popolazione distinta, per la quale non necessariamente è valido quando noto per le donne con mutazione.
Dottor Girardi, la differenza tra Angelina Jolie e i soggetti del vostro studio è che la Jolie aveva fatto un test ed era risultata portatrice di entrambe le mutazioni. Le donne che hanno partecipato alla ricerca invece sono parenti di donne che sono affette dalla mutazione ma che a loro volta sono risultate negative ai test genetici. Come mai è importante condurre uno studio anche su chi è negativo al test?
La negatività del test per BRCA1 e BRCA2 non necessariamente equivale a “rischio assente”. I partecipanti allo studio (tutte familiari di portatrici) appartengono comunque a famiglie ad alto rischio nelle quali ulteriori mutazioni in geni minori (che co-segregano con BRCA1 e BRCA2) potrebbero essere presenti (SNPs, vedi sopra). Tali mutazioni potrebbero potenzialmente “passare” ai negativi al test (le partecipanti allo studio) pur in assenza di mutazione BRCA1 o BRCA2. Questa era l’ipotesi alla base di alcuni studi che mostravano un rischio aumentato di tumore mammario o ovarico (fino a 2-5 volte superiore!) nei “predictive test negatives”. Altri studi tuttavia non confermavano tali risultati. Tutti gli studi furono condotti in gruppi di individui relativamente piccoli. Pertanto la definizione del rischio rappresentava un’area di incertezza. Il nostro studio e’ stato condotto nella piu’ grande popolazione ad oggi e aveva lo scopo di chiarire il quesito. Quali sono le conseguenze di non riuscire a definire il rischio? (1) Donne con test negativo per la mutazione di famiglia potrebbero essere falsamente rassicurate; (2) donne non testate potrebbero sottoporsi a indagini diagnostiche o a chirurgia preventiva demolitiva in assenza di beneficio e con chiaro impatto fisico, estetico e psicologico.
Nella sua esperienza clinica o di ricerca ci sono donne che si sottopongono alla chirurgia preventiva pur non essendo portatrici?
Quale oncologo medico non ho esperienza clinica nel counselling genetico. Ho svolto lo studio in qualità di epidemiologo. I dati dello studio mostravano che una quota di donne inserite in EMBRACE si sottoponeva a mastectomia bilaterale od ovariectomia bilaterale in assenza di diagnosi oncologica e prima del test genetico. Si può pertanto sospettare che questi fossero interventi chirurgici profilattici. Tuttavia non vi è la certezza poiché non avevamo notizia di diagnosi non oncologiche (es. fibromatosi uterina). È bene specificare che tali individui, pur reclutati in EMBRACE (EMBRACE arruola portarici e familiari) non sono stati inclusi nel mio studio perché non più a rischio (essendo stati asportati chirurgicamente mammelle e/o ovaie).
In che modo questo studio potrebbe cambiare l’approccio nella prevenzione al cancro al seno o al tumore ovarico in donne che hanno una familiarità con quelle forme tumorali?
Il nostro studio ha stabilito con un buon livello di confidenza, considerata la dimensione del campione, che individui privi della mutazione familiare BRCA1 o BRCA2 (“predictive test negatives“) non dovrebbero essere candidate a chirurgia preventiva solo sulla base della storia familiare. Non presentato cioè un livello di rischio di sviluppare tumore mammario od ovarico tale da giustificare procedure chirurgiche profilattiche secondo le linee guida più recenti (trattandosi di Regno Unito ci siamo riferiti quelle del National Institute for Health and Care Excellence). Tuttavia, tali individui potrebbero ancora beneficiare di sorveglianza personalizzata (mammografie più frequenti o risonanza magnetica) in presenza di altri fattori di rischio (alcune lesioni istologiche predisponenti o familiari con storia di neoplasia nel braccio di famiglia non portatore della lesione). Lo studio non ha potuto chiarire ulteriormente poiché la storia familiare dettagliata non era disponibile (per questo abbiamo condotto alcune simulazioni per confermare la validità dei nostri risultati). Il modello predittivo BOADICEA consente di avere una stima dettagliata del rischio.
Ci sono dei rischi nella chirurgia preventiva basandosi solo sui risultati dei test genetici sia che siano positivi che negativi? È più prudente tenere conto anche di altri fattori di rischio specifico?
Il rischio intrinseco all’intervento è quello proprio di ogni intervento di chirurgia maggiore. Il rischio aggiuntivo di praticare una chirurgia profilattica non necessaria e’ quello di produrre potenzialmente conseguenze estetiche, psicologiche e sessuali irreversibili o solo parzialmente reversibili. Fattori di rischio ulteriori vanno sempre considerati e la decisione finale deve essere sempre essere concertata con la paziente. Tale decisione tuttavia dovrebbe basarsi sull’evidenza scientifica disponibile. I risultati del nostro studio sono stati ottenuti a livello di popolazione. Per quanto possano essere traslati, in linea di principio, al singolo individuo, il bilancio finale di vantaggi e rischi e’ sempre di natura individuale.
In base ai risultati dello studio quale è la strada migliore da percorrere per una donna che sa di avere dei familiari con la mutazione sui due geni ma che al tempo stesso è negativa al test genetico?
Ciò che si può concludere sulla base dello studio è che una donna appartenente a una famiglia con mutazione BRCA1 o BRCA2 dovrebbe sempre rivolgersi a un genetista clinico per un percorso di counselling. A questo punto dovrebbe sottoporsi al test predittivo e, se negativo, non sottoporsi a chirurgia profilattica. Tuttavia non è escluso che, in presenza di fattori di rischio addizionali, debba sottoporsi a sorveglianza personalizzata. È importante sottolineare che il test genetico dovrebbe costituire sempre la base per ogni decisione. L’uso di algoritmi predittivi quali BOADICEA è anche consigliato, per avere una stima più dettagliata del rischio potenziale.
Foto copertina via